Erwin
Well-Known Member
Hallo,
Ich weiß das ist zuviel Urea, aber mal rein theoretisch.
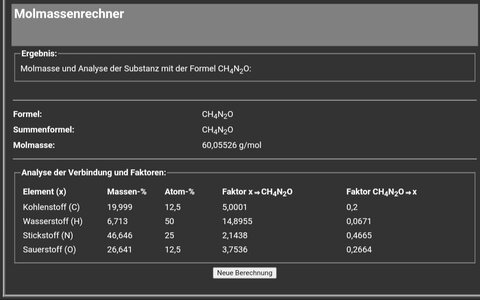
Wenn ich 1g Urea in 100 Liter Wasser gebe entspricht dies laut Nährstoffrechner 10mg/l Urea und daraus entstehen dann 20,6mg/l Nitrat.
Angenommen das ganze Urea wird zu Nitrat umgesetzt.
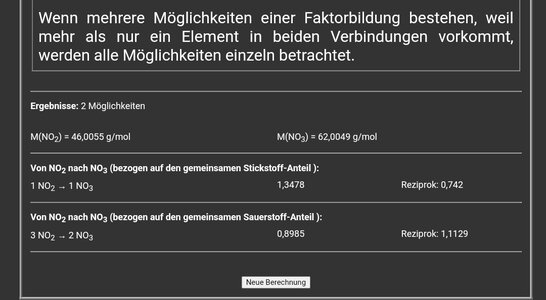
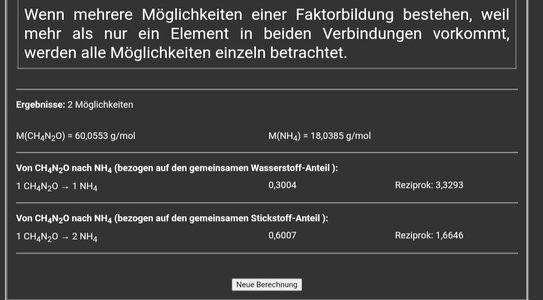
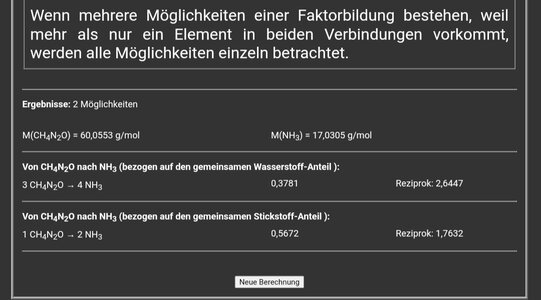
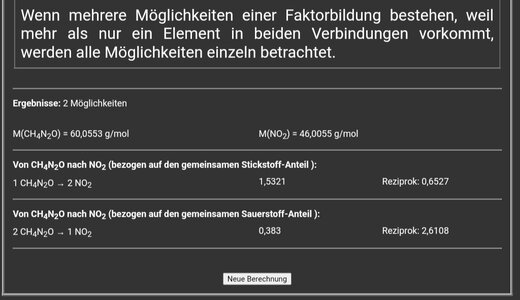
Wie wäre dann die maximale Menge der (kurzfristig) entstehenden Zwischenprodukte Ammonium (eventuell auch Ammoniak) und Nitrit?
Oder anders:
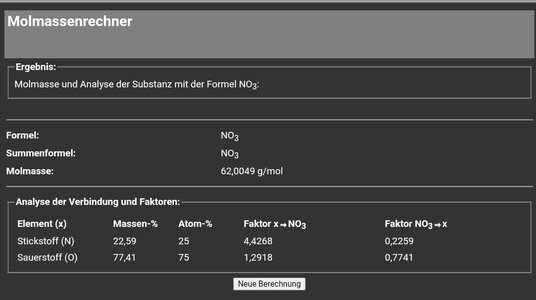
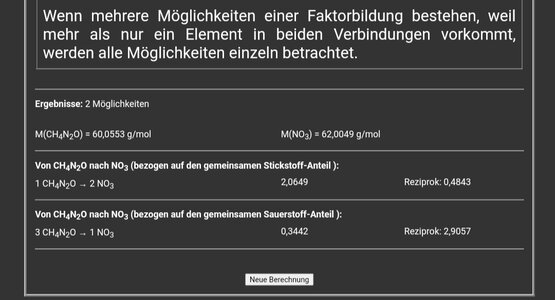
Aus 1g Urea (können) entstehen 2,06g Nitrat....
Aus 1g Urea (können) entstehen wieviel....
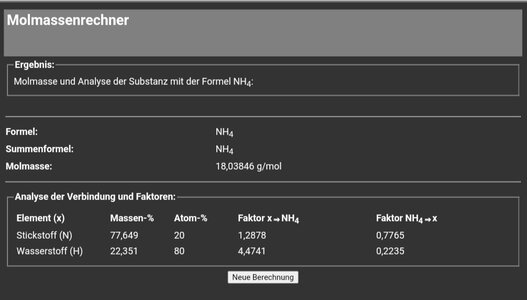
-a; Ammonium
-b; Ammoniak
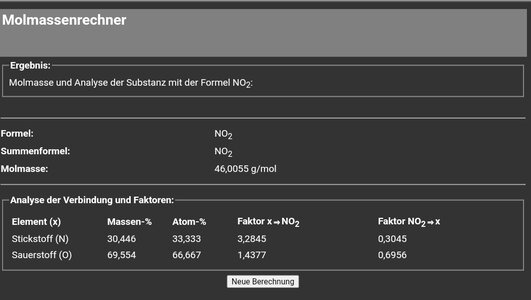
-c; Nitrit
MfG
Erwin
Ich weiß das ist zuviel Urea, aber mal rein theoretisch.
Wenn ich 1g Urea in 100 Liter Wasser gebe entspricht dies laut Nährstoffrechner 10mg/l Urea und daraus entstehen dann 20,6mg/l Nitrat.
Angenommen das ganze Urea wird zu Nitrat umgesetzt.
Wie wäre dann die maximale Menge der (kurzfristig) entstehenden Zwischenprodukte Ammonium (eventuell auch Ammoniak) und Nitrit?
Oder anders:
Aus 1g Urea (können) entstehen 2,06g Nitrat....
Aus 1g Urea (können) entstehen wieviel....
-a; Ammonium
-b; Ammoniak
-c; Nitrit
MfG
Erwin